Elementen kunnen als beide worden geclassificeerd metalen of niet-metalen gebaseerd op hun eigenschappen. Vaak kun je zien dat een element een metaal is door simpelweg naar de metalen glans te kijken, maar dit is niet het enige onderscheid tussen deze twee algemene groepen elementen.
Metalen
De meeste elementen zijn metalen. Dit omvat de alkalimetalen, aardalkalimetalen, overgangsmetalen, lanthaniden en actiniden. Op de periodiek systeemmetalen worden van niet-metalen gescheiden door een zigzaglijn die door koolstof, fosfor, selenium, jodium en radon loopt. Deze elementen en die rechts ervan zijn niet-metalen. Elementen links van de regel kunnen worden genoemd metalloïden of halfmetalen en hebben eigenschappen die tussenliggen tussen die van de metalen en niet-metalen. De fysische en chemische eigenschappen van de metalen en niet-metalen kunnen worden gebruikt om ze van elkaar te onderscheiden.
Metaal fysische eigenschappen:
- Glanzend (glanzend)
- Goed geleiders van warmte en elektriciteit
- Hoog smeltpunt
- Hoge dichtheid (zwaar voor hun formaat)
- Buigzaam (kan worden gehamerd)
- Nodulair (kan in draden worden getrokken)
- Meestal stevig bij kamertemperatuur (een uitzondering is kwik)
- Ondoorzichtig als een dun vel (kan niet door metalen heen kijken)
- Metalen zijn sonoor of maken een belachtig geluid wanneer ze worden geraakt
Metaal chemische eigenschappen:
- Heb 1-3 elektronen in de buitenste schil van elk metaalatoom en verlies gemakkelijk elektronen
- Gemakkelijk corroderen (bijv. Beschadigd door oxidatie zoals aanslag of roest)
- Verlies gemakkelijk elektronen
- Vorm basische oxiden
- Favoriet lagere elektronegativiteiten
- Zijn goede reductiemiddelen
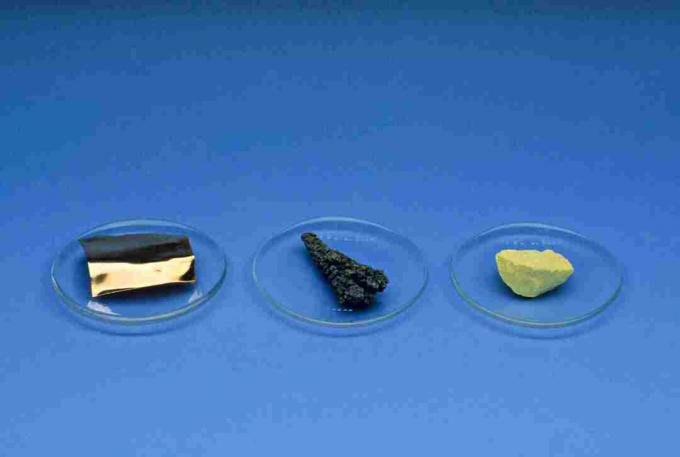
Niet-metalen
Niet-metalen, met uitzondering van waterstof, bevinden zich aan de rechterkant van het periodiek systeem. Elementen die niet-metalen zijn, zijn waterstof, koolstof, stikstof, fosfor, zuurstof, zwavel, selenium, alle halogenen en de edelgassen.
Niet-metalen fysieke eigenschappen:
- Niet glanzend (saai uiterlijk)
- Slechte geleiders van warmte en elektriciteit
- Niet-geleidbare vaste stoffen
- Brosse vaste stoffen
- Dit kunnen vaste stoffen, vloeistoffen of gassen zijn bij kamertemperatuur
- Transparant als een dun vel
- Niet-metalen zijn niet sonoor
Niet-metalen chemische eigenschappen:
- Meestal hebben ze 4-8 elektronen in hun buitenste schil
- Verkrijg of deel valentie-elektronen
- Vorm zure oxiden
- Hebben hogere elektronegativiteiten
- Zijn goed oxidatiemiddelen
Zowel metalen als niet-metalen nemen verschillende vormen aan (allotropen), die verschillende vormen en eigenschappen van elkaar hebben. Grafiet en diamant zijn bijvoorbeeld twee allotropen van de niet-metalen koolstof, terwijl ferriet en austeniet twee allotropen van ijzer zijn. Hoewel niet-metalen een allotroop hebben die metaalachtig lijkt, zien alle allotropen van metalen eruit als wat we beschouwen als een metaal (glanzend, glanzend).